Tratamiento con VYONDYS 53 (golodirsén).
La falta de distrofina hace que las células musculares se dañen y se debiliten con el tiempo.
VYONDYS 53 utiliza tecnología de omisión de exones para permitir que el cuerpo produzca una forma más corta de la proteína distrofina en algunos pacientes omitiendo un exón específico en el gen de la distrofina.
Conozca a Nicholas, de 17 años de edad,
susceptible a la omisión del exón 53
“La prueba genética del paciente con la enfermedad de Duchenne identificó que tenía una mutación que podría tratarse con VYONDYS 53. Su médico dijo que era susceptible a recibir tratamiento con la terapia de omisión de exones”.
¿Qué es la omisión de exones?
La enfermedad de Duchenne es causada por una mutación genética en el gen de la distrofina. Con mayor frecuencia, faltan uno o más exones (partes del gen), lo que causa errores en las instrucciones para producir distrofina. Esto hace que el cuerpo no pueda producir suficiente o ninguna proteína distrofina funcional. El objetivo de la omisión del exón es permitir que el cuerpo produzca una forma más corta de la proteína distrofina. Este vídeo le mostrará cómo.
Cómo funciona la omisión de exones.
Comprender el gen de la distrofina.
El gen de la distrofina está compuesto por exones (partes de un gen) que están unidos para proporcionar instrucciones para producir distrofina, una proteína que nuestros músculos necesitan para funcionar correctamente. Sin distrofina, las células musculares se dañan y debilitan con el tiempo.

Cómo se conectan los exones.
Con 79 exones, el gen de la distrofina es el más grande del cuerpo. Piense en los exones del gen de la distrofina como los vagones de tren de juguete, cada uno con una conexión especial que permite que un vagón se conecte con otro. Para que todos los vagones se muevan juntos como un tren, las conexiones entre los vagones deben coincidir, por ejemplo, de círculo a círculo y de cuadrado a cuadrado.
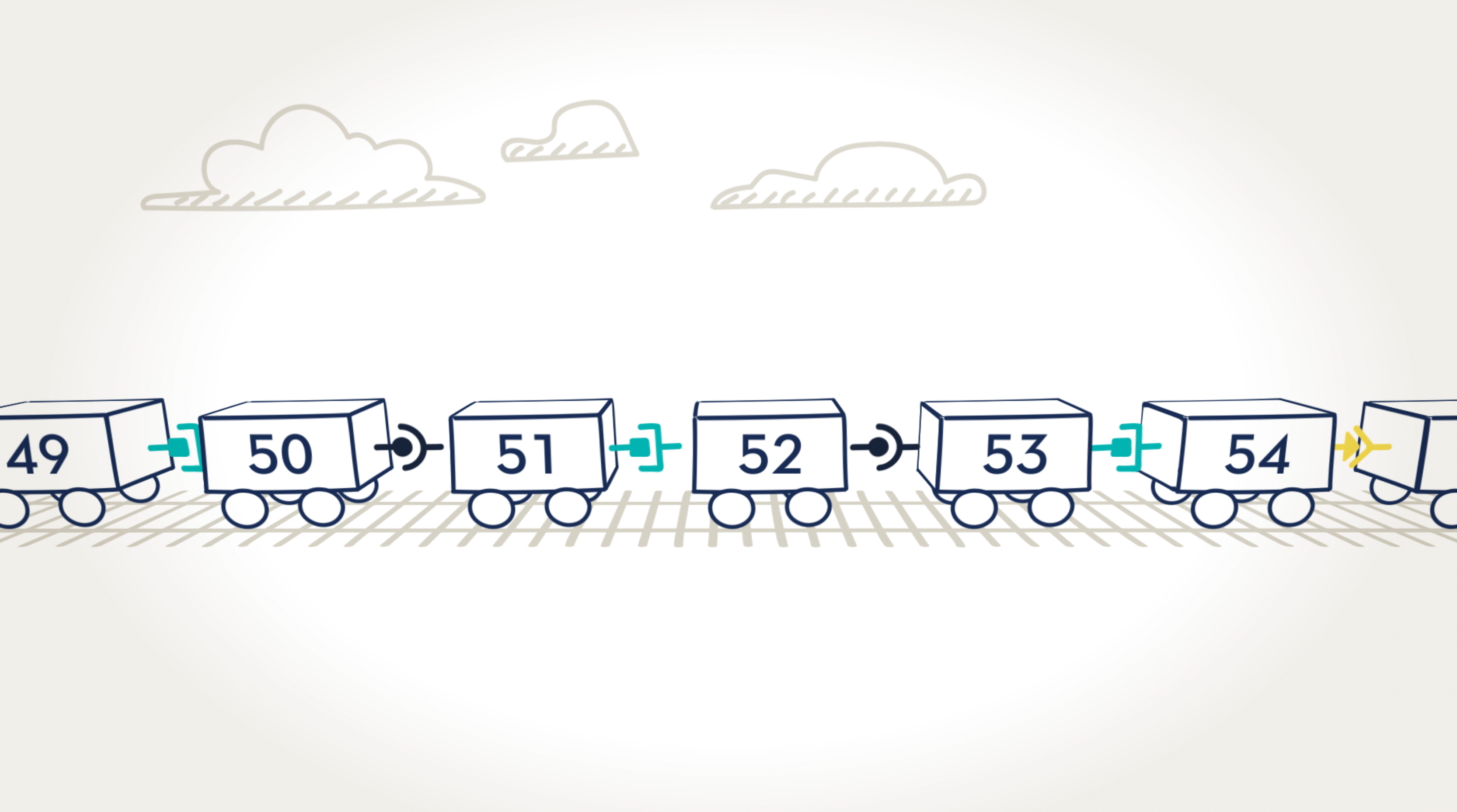
Cuando falta un exón.
Aquí podemos ver que faltan los vagones, o exones, 50, 51 y 52. El resultado es que los vagones 49 y 53 no pueden conectarse porque sus conectores son de formas diferentes y no encajan entre sí. En el gen de la distrofina, este exón ausente impediría que el cuerpo pueda leer las instrucciones para fabricar la proteína distrofina.

Omisión de los exones.
Al dejar a un lado ciertos exones, o vagones, podemos “omitirlos” para encontrar un vagón con el conector adecuado. El nuevo tren sería más corto, pero los vagones están conectados. Al igual que hemos omitido un vagón de tren, VYONDYS 53 está diseñado para omitir un exón.

El resultado: una forma más corta de distrofina.
VYONDYS 53 funciona con tecnología de omisión de exones. En algunos niños varones, se ha demostrado que las infusiones semanales con VYONDYS 53 ayudan al organismo a producir una forma más corta de la proteína distrofina. Vea el video.

Los estudios clínicos de VYONDYS 53 analizaron si la omisión del exón se producía en el gen de la distrofina de los niños varones tratados con el fármaco. En esos estudios, se produjo una omisión del exón en los 25 participantes del estudio evaluados. Los niños varones que recibieron VYONDYS 53 tuvieron respuestas variables en la cantidad de producción de distrofina.

FAQs Relacionadas
Los pacientes con la enfermedad de Duchenne que reciban VYONDYS 53 deben someterse a una prueba genética que muestre una mutación en el gen de la distrofina que pueda tratarse mediante la omisión del exón 53. El médico de su hijo está mejor equipado para determinar si la mutación de su hijo es susceptible al tratamiento con VYONDYS 53. Hemos desarrollado una Guía para hablar con el médico para ayudarle a iniciar esa importante conversación.
Sí. VYONDYS 53 se ha estudiado en ensayos clínicos. Vea los resultados de los ensayos clínicos.
